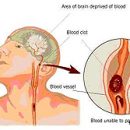
Până în prezent, leziunea cerebrală (CMT) este una dintre cele mai frecvente tipuri de patologie neurologică și este o problemă medicală și socio-economică semnificativă pentru toate segmentele populației.
Conţinut
În țările dezvoltate, există o creștere constantă a neurotraumamismului. Deci, în țările Europei, 150 este înregistrată anual–300 de cazuri de CHMT la 100 mii. Populație. În SUA, doar 2003. A menționat mai mult de 1,5 milioane cmt. În Rusia, această cifră ajunge la 4 cazuri la 1 mii. Uman. Cea mai importantă problemă din punct de vedere medical este că un număr semnificativ de victime dezvoltă ulterior așa-numitele consecințe ale CMT amânat, adesea interpretate în encefalopatia post-traumată. Printre cele mai frecvente sindroame care determină nivelul de adaptare socio-gospodăriile și calitatea vieții pacienților sunt încălcări unice intelectuale. Tulburările cognitive post-traumatice sunt izolate în 29,4% din toți pacienții cu consecințe ale CHMT și în combinație cu alte sindroame — Y 35,7%. În general, printre consecințele tulburărilor cognitive amânate CMT ca sindrom se găsesc în 65,1% din cazuri.
Patogeneza dezvoltării tulburărilor cognitive post-traumante este foarte complexă și multilaterală. Ca principalii factori care pot duce la formarea unui deficit cognitiv în perioada acută, considerăm atât daune mecanice directe asupra țesuturilor creierului, cât și a efectului mediate al anumitor procese fiziopatice care apar din CHT, cum ar fi umflarea umflării creierului, întreruperea lichiorului, hemodinamică și dr. În același timp, se știe că în ceea ce privește cazurile de tulburare a funcțiilor de masă intelectuală, este conservată o perioadă lungă de timp sau este un caracter persistent. La alți pacienți, ele apar în perioada îndepărtată de rănire și au o tendință distinctă față de progresie. Mecanismul apariției unor astfel de încălcări nu rămâne studiat în remediu. Datele obținute sugerează că factorii patologici afectează celula nervoasă în perioada acută, contribuie la apariția unei cascade de schimburi biochimice în neuroni, ceea ce duce la dezvoltarea proceselor distrofice și la reducerea eficacității transmisiei sinaptice.
În cele din urmă, există o încălcare a proceselor de diseminare a informațiilor în rețelele neuronale, considerate ca fiind unul dintre principalele aspecte ale formării încălcărilor cognitive. Un număr de cercetători notează o anumită similitie a mecanismelor patogenetice pentru dezvoltarea tulburărilor cognitive la leziunile creierului CMT și vasculare. În plus, un posibil rol al leziunii cerebrale este prezentat ca un lansator al bolilor neurodegenerative, în special boala Alzheimer. În prezent, mai multe procese patofiziologice joacă un rol semnificativ în formarea tulburărilor cognitive post-traumante.
Unul dintre aceste procese este dezvoltarea «Exaitotoxicitatea glutamatică». În condiții fiziologice, glutamatul acționează ca unul dintre cei mai importanți mediatori interesanți ai sistemului nervos central, care participă la punerea în aplicare a proceselor de plasticitate neuronală și funcțiile integrative ale creierului. O cantitate semnificativă de receptori glutamantherme este observată la cortexul cerebral și la hipocamp. În același timp, cu patologie, se observă emisiile de glutamat excesive, care în aceste condiții are un efect toxic asupra structurilor neuronale, care contribuie la activarea reacțiilor cascadă de glutamat-calciu, ceea ce duce la o creștere necontrolată a concentrației de calciu intracelular , care are un efect negativ asupra aprovizionării cu energie celulară. Se arată că, în condițiile de ischemie în țesuturi, există o creștere semnificativă a nivelului de formare a radicalilor liberi, care contribuie, de asemenea, la excesul de acumulare intracelulară de calciu.
Creierul este foarte sensibil la acțiunea radicalilor liberi. În condițiile predominanței sistemelor oxidante față de antioxidant, formarea așa-numitului stres oxidant. În acest caz, hidroliza fosfolipazei este activată și membranele celulare sunt degradarea, inclusiv mitocondrialul. Eliminarea tulburărilor emergente este o condiție prealabilă pentru gestionarea cu succes a pacienților cu insuficiență cognitivă post-traumică. Cu aceste poziții, este oportună numirii unui astfel de medicament ca o noopept cu astfel de proprietăți. Noopept — N-fenil-acetil-L-prolyglicine ester etilic — Noua dipeptidă originală internă creată în farmacologie. ÎN.ÎN.Zasakova Ramne. Potrivit datelor obținute în cursul studiilor experimentale, Nopept are proprietăți nootropice și neuroprotectorive. Medicamentul în caracteristicile sale constante structurale este similar cu piracetam și vasopresina. Dezvoltarea acestui medicament a fost efectuată ca parte a ideii existente că unele peptide de reglementare au un impact semnificativ asupra mecanismelor de memorie și de formare.
Baza explicației acțiunii de NOOPEPT este o ipoteză că medicamentul de bază al acestui grup de piracetam este un analog al unui ligand peptidic la receptori nominali specifici, similar cu caracteristicile sale cu metaboliți de vasopresină. NOOPEPT este benefică din vasopresină, deoarece este capabilă să prezinte activitatea cu administrarea sistemică, inclusiv a administrației orale. În timpul studiilor, sa arătat biodisponibilitatea ridicată a medicamentului pentru țesuturile cerebrale, precum și toxicitatea redusă. Studiul în experimentul pe animalele de laborator a făcut posibilă stabilirea faptului că utilizarea dozelor de medicament, de la 2 la 20 de ori mai mare decât nootropic, nu provoacă daune organelor interne, nu are încălcări semnificative ale indicatorilor hematologici și biochimici. La efectuarea unui număr de studii clinice, se arată și siguranța ridicată a medicamentului și tolerabilitatea sa bună. În cursul cercetării, sa constatat că NOOPEPT are un mecanism cuprinzător de acțiune.
În primul rând, are un efect notropic asociat cu faptul că unul dintre metaboliții activi ai NOOPEPT este cicloprolglicina, care, în structura sa, este similar cu o dippotidă ciclică endogenă, care are activitate anti-informică.
În al doilea rând, NOOPEPT este capabil să crească stabilitatea țesutului cerebral la impactul dăunător, cum ar fi leziunea hipoxică, electrosusculară și toxică, care caracterizează efectul neuroprotector al acestui medicament. În al treilea rând, se arată posibilitatea unei nodopept pentru a preveni în condițiile acțiunilor concentrațiilor toxice de glutamat și a formelor active de deces de oxigen a neuronilor în corpul cortexului cortexului cerebral și cerebelul cerebral. În plus, experimentul a evidențiat capacitatea de a reduce efectul toxic al b-amiloidului, de a spori producția de anticorpi anti-mylide, modularea funcționării receptorilor colinergici, precum și stimularea expresiei factorilor neurotrofici (BDNF și NGF) în Cortexul cerebral și hipocamp.
Relevanța problemei încălcărilor cognitive post-traumatice, valabilitatea utilizării de NOUPEPT, ținând seama de prezența unui punct de aplicare la nivel neurochimic, sub consecințele CHT, precum și preliminarul, inclusiv experimental și Eficacitatea clinică a medicamentului a fost motivul acestui studiu.
Scopul studiului a fost de a evalua eficacitatea, precum și siguranța utilizării medicamentului NOOPEPT la pacienții cu tulburări cognitive post-traumante. Studiul a fost realizat pe un protocol special dezvoltat și a respectat toate cerințele privind practica clinică adecvată (GCP) adoptată în Federația Rusă. Studiul a inclus pacienți care îndeplinesc criteriile de includere, după semnarea obligatorie a consimțământului informat.
30 de pacienți cu vârsta de 19 ani au participat la studiu–66 de ani (vârsta medie 33±10,3 ani), care a suferit o CHAH (creier de contuzie sau leziune a unui grad de lumină) în urmă și având o întrerupere a funcțiilor de masă intelectuală asociată cu această stare corespunzătoare criteriilor pentru sindromul tulburărilor cognitive moderate. Toți pacienții au corespuns criteriilor de sindromul încălcărilor cognitive moderate, iar tulburările lor cognitive au fost inițial evaluate în 25 sau mai multe puncte pe scala de examinare de stat mini-mental (MMSE).
Excepții Criteriile de cercetare au fost: prezența bolilor somatice concomitente sau instabile care amenință viața pacientului, prezența altcinelor semnificative din punct de vedere clinic (cu excepția sindromului încălcărilor cognitive moderate cu consecințele CHF) tulburărilor neurologice sau mentale, Prezența unui motor grosier sau a unui defect senzorial sau a altor tulburări care au făcut dificilă realizarea unui studiu neuropsihologic sau a altor studii prevăzute de protocol, o istorie a accidentului vascular cerebral sau a encefalopatiei discirculatoare etapa III, terapie simultană cu alte vasoactive, Medicamente metabolice sau psihotrope cu efect stimulator cognitiv dovedit, intoleranță la medicamentul în studiu, perioada de sarcină și lactație.
Atunci când efectuați lucrări pentru obiecționarea datelor obținute au fost aplicate
Următoarele metode:
1) evaluarea statutului neurologic;
2) o scară scurtă a stării mentale — MMSE;
3) scale Hamilton pentru a evalua depresia;
4) Bateria de testare pentru disfuncția frontală — Baterie de evaluare frontală (FAB);
5) urmăriți testul desenului;
6) Testați 10 cuvinte;
7) Procesul Schulte;
8) Scala de evaluare a unei impresii clinice generale de schimbare — Clinician’S impresia bazată pe interviu a schimbării plus (cibic plus);
9) Metode de neurovasualizare: Tomografie de rezonanță magnetică sau magnetică.
Evaluarea pe o scară a unei experiențe clinice generale prevăzută pentru o evaluare a stării pacientului la terapia și evaluarea severității modificărilor în contextul tratamentului. Medicul de participare înainte de începerea tratamentului a făcut o evaluare a stării pacientului pe baza unei analize a tulburărilor pe o scară de 7 puncte, estimând imaginea clinică a bolii, monitorizarea pacientului, starea sferei mentale a Pacient, comportament, starea funcțiilor socio-interne.
La începutul studiului, a fost efectuată o vizită de screening, pe care conformitatea pacientului a fost determinată de criteriile de includere. Apoi, în cazul conformității pacientului, protocolul a semnat consimțământul informat. Această vizită a evaluat, de asemenea, rezultatele electrocardiogramelor, metodelor de laborator și neurovalizării de cercetare. După aceea, a fost estimată statutul neurologic, testarea neuropsihologică de bază a fost efectuată pentru a determina nivelul inițial al stării cognitive.
Începând cu a doua zi a vizitei de screening, pacienții au primit un NOOPEPT timp de 10 mg de 2 ori pe zi timp de 60 de zile. În viitor, evaluarea eficacității terapiei a fost efectuată în zilele 30 și 60 de tratament. Planul evenimentelor este prezentat în tabel.
În studiul nostru, perioada medie după prejudiciul suferit a fost de 7±3,8 ani. Toți cei 30 de pacienți care au intrat în studiu au avut inițial încălcări ușoare pe scara impresiei clinice generale a schimbării (Cibic Plus). În timpul unei vizite de screening, toți pacienții examinați au prezentat plângeri cu privire la reducerea memoriei, concentrarea atenției, reducerea eficacității activităților zilnice, slăbiciune generală, a crescut oboseala. În plus, unii dintre pacienți au prezentat alte plângeri: la cefalee (43,3%), dificultăți cu planificarea diferitelor activități (40%), tulburare de somn (26,7%), instabilitatea dispoziției (23,3%). În timpul examinării neurologice a încălcărilor brute nu a fost detectată. La 53,3% dintre pacienți, au existat simptome împrăștiate sub formă de microiimptomi izolați, 13,3% — Încălcarea coordonatorului de lumină. La același număr de reflexe plastice patologice bilaterale observate (Rossolimo, Vartenberg). Toți pacienții aveau semne de sindrom astemic. 53,3% au observat semne de instabilitate vegetativă-vasculară.
Studiul funcțiilor cognitive ale pacienților efectuate în dinamica a arătat că, prin rezultatele scalei MMSE, diferențele fiabile cu nivelul inițial au fost prezentate la 30 de zile după începerea tratamentului. În special, înainte de admiterea medicamentului, scorul mediu a fost de 26,5±0,94; 1 lună de la începutul terapiei — 27.6±0,99 puncte (p<0,01). În același timp, 60 de zile de la începutul terapiei, scorul mediu pe această scară a fost de 27,7±1.09, care a caracterizat absența unei îmbunătățiri suplimentare (P>0,05) și a fost afișată doar o tendință de reducere a tulburărilor cognitive. Dinamica indicatorilor neuropsihologici pe scara MMSE este prezentată în orez. unu.
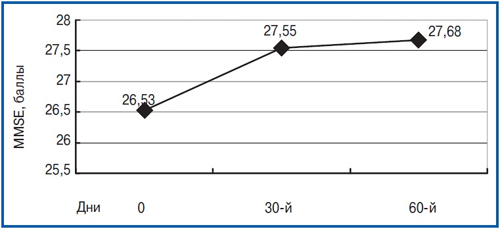
Imaginea 1
Interesant a fost faptul că în structura scalei MMSE, cea mai semnificativă îmbunătățire a indicatorilor a fost obținută de subshkale «Atenţie», caracterizând într-o anumită măsură starea proceselor neurodinamice care suferă de TBMC (P<0,01), precum și pe subshkale «memorie» (R<0,05). Pe scara bateriei testelor pentru a evalua disfuncția frontală a diferențelor fiabile Fab asupra perioadei de observare din dinamica nu a fost disponibilă (la vizita inițială — 15.9±0,78 puncte, 60 de zile mai târziu — 16,8±0,87, p = 0,27). Testul testului de desen al ceasului cu o estimare de 10 puncte asupra vizitei sursă este de obicei estimat la 9–10 puncte și în contextul tratamentului modificărilor semnificative nu au fost supuse. Desigur, datele obținute pe baza evaluării rezultatelor eșantionului Schulte, care a fost efectuată pe toate cele 3 vizite. Eșantionul estimat cuprinzător, utilizând 5 mese de pacienți prezentate consecutiv, vă permite să caracterizați astfel de modificări neurodinamice ca o deteriorare a concentrației de atenție, creșterea epuizării proceselor mentale și a atenției instabilității. Aceste modificări într-o anumită măsură au fost caracterizate de majoritatea pacienților la vizite de screening. Timpul mediu de testare pentru fiecare dintre cele cinci prezentări din prima vizită a fost de 45,5±6.24 S. După 2 luni de la începutul terapiei, timpul a scăzut la 40.2±5.20 s, care a caracterizat o îmbunătățire semnificativă a concentrației de atenție (p<0,05). Dinamica timpului de eșantion al Schulte este prezentată în orez. 2.
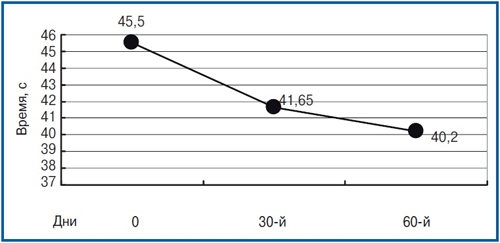
Figura 2
După cum se poate vedea din graficul din orez. 2, cea mai semnificativă reducere în timpul petrecut pe execuția probelor a fost demonstrată de pacienți la 30 de zile de la începutul terapiei. Recunoașterea dinamicii pozitive a persistat și în luna a doua a medicamentului și a fost caracterizată printr-o scădere și mai pronunțată a timpului de testare cu o stabilizare mai puțin semnificativă a îmbunătățirii decât pe scala MMSE.
Evaluarea pe o scară a unei experiențe clinice generale prevăzută pentru o evaluare a stării pacientului la terapia și evaluarea severității modificărilor în contextul tratamentului. Medicul de participare înainte de începerea tratamentului a făcut o evaluare a stării pacientului pe baza unei analize a tulburărilor pe o scară de 7 puncte, estimând imaginea clinică a bolii, monitorizarea pacientului, starea sferei mentale a Pacient, comportament, starea funcțiilor socio-interne.
La începutul studiului, a fost efectuată o vizită de screening, pe care conformitatea pacientului a fost determinată de criteriile de includere. Apoi, în cazul conformității pacientului, protocolul a semnat consimțământul informat. Această vizită a evaluat, de asemenea, rezultatele electrocardiogramelor, metodelor de laborator și neurovalizării de cercetare. După aceea, a fost estimată statutul neurologic, testarea neuropsihologică de bază a fost efectuată pentru a determina nivelul inițial al stării cognitive.
Începând cu a doua zi a vizitei de screening, pacienții au primit un NOOPEPT timp de 10 mg de 2 ori pe zi timp de 60 de zile. În viitor, evaluarea eficacității terapiei a fost efectuată în zilele 30 și 60 de tratament. Planul evenimentelor este prezentat în tabel.
| Metode de cercetare | I | II | III |
| fundal | A 30-a zi | Ziua 60 a | |
| Colecția de evaluare a stării mentale (MMSE) | V | V | V |
| Evaluarea disfuncției frontale (FAB) | V | V | |
| Testați orele de desen 10 – Estimarea palleală | V | V | |
| Scala impresiei clinice generale (CGI) | V | V | |
| Testați 10 cuvinte | V | V | |
| Exemplu Schulte | V | V | V |
| Scala Hamilton | V | ||
| Evaluarea fenomenelor nedorite și a efectelor secundare | V | V |
Figura 3
În studiul nostru, perioada medie după prejudiciul suferit a fost de 7±3,8 ani. Toți cei 30 de pacienți care au intrat în studiu au avut inițial încălcări ușoare pe scara impresiei clinice generale a schimbării (Cibic Plus). În timpul unei vizite de screening, toți pacienții examinați au prezentat plângeri cu privire la reducerea memoriei, concentrarea atenției, reducerea eficacității activităților zilnice, slăbiciune generală, a crescut oboseala. În plus, unii dintre pacienți au prezentat alte plângeri: la cefalee (43,3%), dificultăți cu planificarea diferitelor activități (40%), tulburare de somn (26,7%), instabilitatea dispoziției (23,3%). În timpul examinării neurologice a încălcărilor brute nu a fost detectată. La 53,3% dintre pacienți, au existat simptome împrăștiate sub formă de microiimptomi izolați, 13,3% — Încălcarea coordonatorului de lumină. La același număr de reflexe plastice patologice bilaterale observate (Rossolimo, Vartenberg). Toți pacienții aveau semne de sindrom astemic. 53,3% au observat semne de instabilitate vegetativă-vasculară.
Studiul funcțiilor cognitive ale pacienților efectuate în dinamica a arătat că, prin rezultatele scalei MMSE, diferențele fiabile cu nivelul inițial au fost prezentate la 30 de zile după începerea tratamentului. În special, înainte de admiterea medicamentului, scorul mediu a fost de 26,5±0,94; 1 lună de la începutul terapiei — 27.6±0,99 puncte (p<0,01). În același timp, 60 de zile de la începutul terapiei, scorul mediu pe această scară a fost de 27,7±1.09, care a caracterizat absența unei îmbunătățiri suplimentare (P>0,05) și a fost afișată doar o tendință de reducere a tulburărilor cognitive. Dinamica indicatorilor neuropsihologici pe scara MMSE este prezentată în orez. unu. Interesant a fost faptul că în structura scalei MMSE, cea mai semnificativă îmbunătățire a indicatorilor a fost obținută de subshkale «Atenţie», caracterizând într-o anumită măsură starea proceselor neurodinamice care suferă de TBMC (P<0,01), precum și pe subshkale «memorie» (R<0,05). Pe scara bateriei testelor pentru a evalua disfuncția frontală a diferențelor fiabile Fab asupra perioadei de observare din dinamica nu a fost disponibilă (la vizita inițială — 15.9±0,78 puncte, 60 de zile mai târziu — 16,8±0,87, p = 0,27). Testul testului de desen al ceasului cu o estimare de 10 puncte asupra vizitei sursă este de obicei estimat la 9–10 puncte și în contextul tratamentului modificărilor semnificative nu au fost supuse.
Desigur, datele obținute pe baza evaluării rezultatelor eșantionului Schulte, care a fost efectuată pe toate cele 3 vizite. Eșantionul estimat cuprinzător, utilizând 5 mese de pacienți prezentate consecutiv, vă permite să caracterizați astfel de modificări neurodinamice ca o deteriorare a concentrației de atenție, creșterea epuizării proceselor mentale și a atenției instabilității. Aceste modificări într-o anumită măsură au fost caracterizate de majoritatea pacienților la vizite de screening. Timpul mediu de testare pentru fiecare dintre cele cinci prezentări din prima vizită a fost de 45,5±6.24 S. După 2 luni de la începutul terapiei, timpul a scăzut la 40.2±5.20 s, care a caracterizat o îmbunătățire semnificativă a concentrației de atenție (p<0,05). Dinamica timpului de eșantion al Schulte este prezentată în orez. 2. După cum se poate vedea din graficul din orez. 2, cea mai semnificativă reducere în timpul petrecut pe execuția probelor a fost demonstrată de pacienți la 30 de zile de la începutul terapiei. Recunoașterea dinamicii pozitive a persistat și în luna a doua a medicamentului și a fost caracterizată printr-o scădere și mai pronunțată a timpului de testare cu o stabilizare mai puțin semnificativă a îmbunătățirii decât pe scala MMSE.